7月22日,山东大学基础医学院于晓教授和孙金鹏教授团队与中科院上海药物研究所谢欣研究员团队、浙江大学张岩研究员团队通力合作,在《Nature》在线发表了题为“Structural basis of GPBAR activation and bile acid recognition”的研究论文。山东大学基础医学院博士后杨帆、肖鹏副教授及博士生郭璐璐、林婧宇、吴襄,浙江大学基础医学院博士后毛春友、明倩倩为共同第一作者;张岩、谢欣、于晓、孙金鹏为共同通讯作者,山东大学为本论文第一单位。
该研究系统地对胆汁酸分子和人工激动剂激活胆汁酸膜受体的过程及受体下游信号转导的偏好性进行了全面详细的探讨,揭示了GPBAR参与胆汁酸识别和其别构效应的独特结构特征,同时阐明了GPCR超家族中配体结合口袋与G蛋白结合位点之间存在着新的激活及相互作用机制。由于GPBAR在代谢和免疫调节中发挥着重要作用,所以GPBAR与激动剂的高分辨率结构以及这些新的发现将促进基于结构的药物设计。
胆汁酸是一类由肝脏细胞产生并由胆管分泌到肠道的两亲性代谢产物,在消化过程中对人体摄入的脂肪有重要的乳化作用。除了正常的乳化作用外,结构多样性的胆汁酸还是重要的体内荷尔蒙,对多种代谢和炎症相关的生理过程有重要的调节作用。现在已知,肝脏可以生成两种初级胆汁酸:胆酸和鹅脱氧胆酸,并在肠道进一步由肠道菌群代谢为多种次级胆汁酸,具有多种不同的生理功能。因此多种多样的胆汁酸与其受体的作用通路构成了肝脏-胆汁酸-肠道菌群重要的信号转导轴,是近期生命医学研究的热点之一。最近一系列研究表明,许多天然胆汁酸和胆汁酸衍生物对原发性硬化性胆管炎(PSC)、非酒精性脂肪性肝炎(NASH)、2型糖尿病和肌萎缩性(脊髓)侧索硬化症(ALS)等神经退行性疾病有治疗作用。在生物体内,胆汁酸可以通过激活核受体FXR和膜受体(GPBAR/TGR5)发挥作用。激活后的GPBAR在不同的病理生理条件下既有好的作用也有坏的作用。例如,胆酸(CA)和牛磺胆酸(TCA)可以增加能量消耗,有益减肥;牛磺脱氧胆酸(TUDCA)一直作为传统中药,发挥抗炎作用并能促进心脏血管舒张。然而,石胆酸(LCA)可引起胰岛素抵抗,脱氧胆酸(DCA)可促进癌症发展。胆汁酸许多有益的作用大都归因于GPBAR与Gs信号途径,如糖尿病的预防、白色脂肪细胞组织褐化、对抗脂肪变性等。最新研究表明,胆汁酸也可以激活arrestin的活性,并介导抗病毒的天然免疫反应。然而,对于GPBAR如何识别不同胆汁酸以及影响下游信号偏好性的机制,其结构基础尚不清楚。
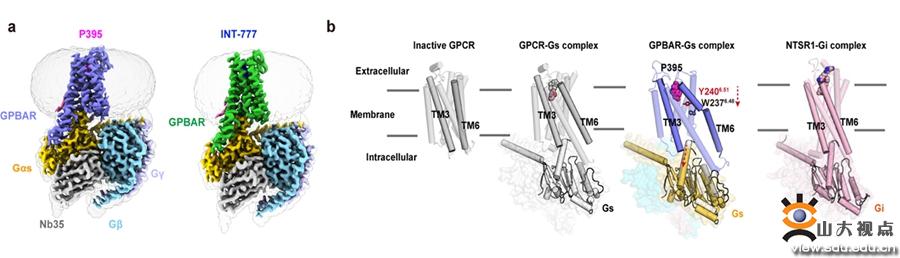
该研究首次利用冷冻电镜单颗粒重构技术解析了胆汁酸受体GPBAR在小分子化合物P395以及胆汁酸类似物INT-777作用下与下游Gs蛋白三聚体形成复合物的高分辨率结构,观察到受体GPBAR对两亲性配体的识别机制,并结合生化和细胞实验阐明了GPBAR识别多种胆汁酸的指纹图谱,阐明了下游偏好性信号途径的结构基础。该研究还发现天然胆汁酸结合受体的第二个别构位点、GPCR激活的新机制以及长期未决的受体第三个内环的功能。
该研究对肝肠轴的信号转导机制研究以及GPCR的激活过程等都将有广泛的影响:一是首次揭示两亲性代谢产物是如何被GPBAR识别并发挥作用的。GPBAR的配体结合口袋中由第五个螺旋及两个胞外环来构成疏水侧面,从而面对胆汁酸的疏水一面,而胆汁酸的另一个亲水结合面则朝向螺旋6和7之间的亲水氨基酸基团,形成特异性的相互作用。二是阐明了胆汁酸受体对多种不同胆汁酸识别的指纹图谱。研究通过对内源性胆汁酸类似物INT-777与GPBAR的结合模式的分析,以及内源性配体CA、DCA、DCA、LCA、TCA、GCA、TDCA、UDCA、TUDCA的配体结合,经过生化及药理学分析,找到了GPBAR识别不同胆汁酸的指纹图谱。这为深入理解胆汁酸的作用机理以及针对于GPBAR的药物设计提供了理论基础。三是发现了第二个胆汁酸在受体上的结合位点。通过电镜结构解析,研究发现了GPBAR存在别构调控位点。研究人员通过对内源性配体的结构及生化数据分析,发现10种胆汁酸中的5个具有12-OH的胆汁酸可以结合在该位点上,并别构调控胆汁酸受体激活的过程。这为理解胆汁酸如何作用于其膜受体的生理过程以及发展和开发别构位点的小分子药物提供了理论基础。四是研究发现胆汁酸受体可以通过Arrestin偏好性途径调控不同的生理功能。通过对结构及生化数据的分析,发现GPBAR的ECL1、ECL3及ICL1是决定配体偏好性的结构基础,这为开发偏好性配体及药物的开发提供了理论基础。五是该研究明确提出了GPBAR非经典的受体激活机制与分子开关。此前“toggle switch”的结合和PIF基序的结构重排都被认为是大多数GPCR的共同机制。而对GPBAR而言,虽然在其第六个跨膜螺旋(TM6)中具有发挥枢纽转换作用的W237氨基酸,但并不具备分子开关功能,发挥分子开关功能的却是其上一个螺旋中的Y240,并且GPBAR的螺旋6与螺旋3的分离程度更大,整个激活模式与结构重排均是一种全新的方式。这些新发现扩展了人们对GPCR激活机制的认识。六是GPCR第三个内环的功能一直不清楚,本研究观察到受体完整清晰的第三个内环密度,首次发现了受体的第三个胞内环可以和Gs蛋白特异性结合,并通过序列比对及生化实验发现,GPCR第三个胞内环与Gs的结合是一个通用的规律,即它们都可以通过细胞内环3偶联基序(R/KψXR/KXψXR)与Gs结合。这些研究阐明了此前尚未了解的GPCR-G蛋白偶联的新机制。
山东大学基础医学院孙金鹏研究团队持续在GPCR跨膜信号转导取得进展,在2015年提出磷酸化编码的笛子模型(Nat Commun. 2015 Sep 8;6:8202.),2017年发现多种GPCR与离子通道偶联的新机制以及介导心血管事件(Nat Commun.2017 Feb 9;8:14335.)(Nature Commun.2018 Jan 2;9:11.)(Elife. 2018 Feb 2;7:e33432.),并发现GPCR通过别构效应调节一大类SH3-CP信号转导蛋白的机制(Nat Chem Biol. 2018 Sep;14(9):876.)。
山东大学基础医学院于晓研究团队关注代谢生理和病理生理中的GPCR,在过去的研究中阐明了胰岛中CRHR2和肾上腺素受体对胰岛环路和稳态的调控作用(J Clin Invest. 2017 Jun 30;127(7):2631)(Diabetologia. 2014 Sep;57(9):1899)(Diabetologia. 2015 Feb;58(2):324), CCK1R偏好性通路对胰岛功能的精确调控机制(Br J Pharmacol. 2015 Nov;172(21):5050),以及粘附类受体对水盐代谢的调控等(Elife. 2018 Feb 2;7:e33432.)。
以上研究得到了国家自然科学基金杰出青年基金和优秀青年基金的资助,该研究同时获得广州中医药大学周玖瑶团队的支持。